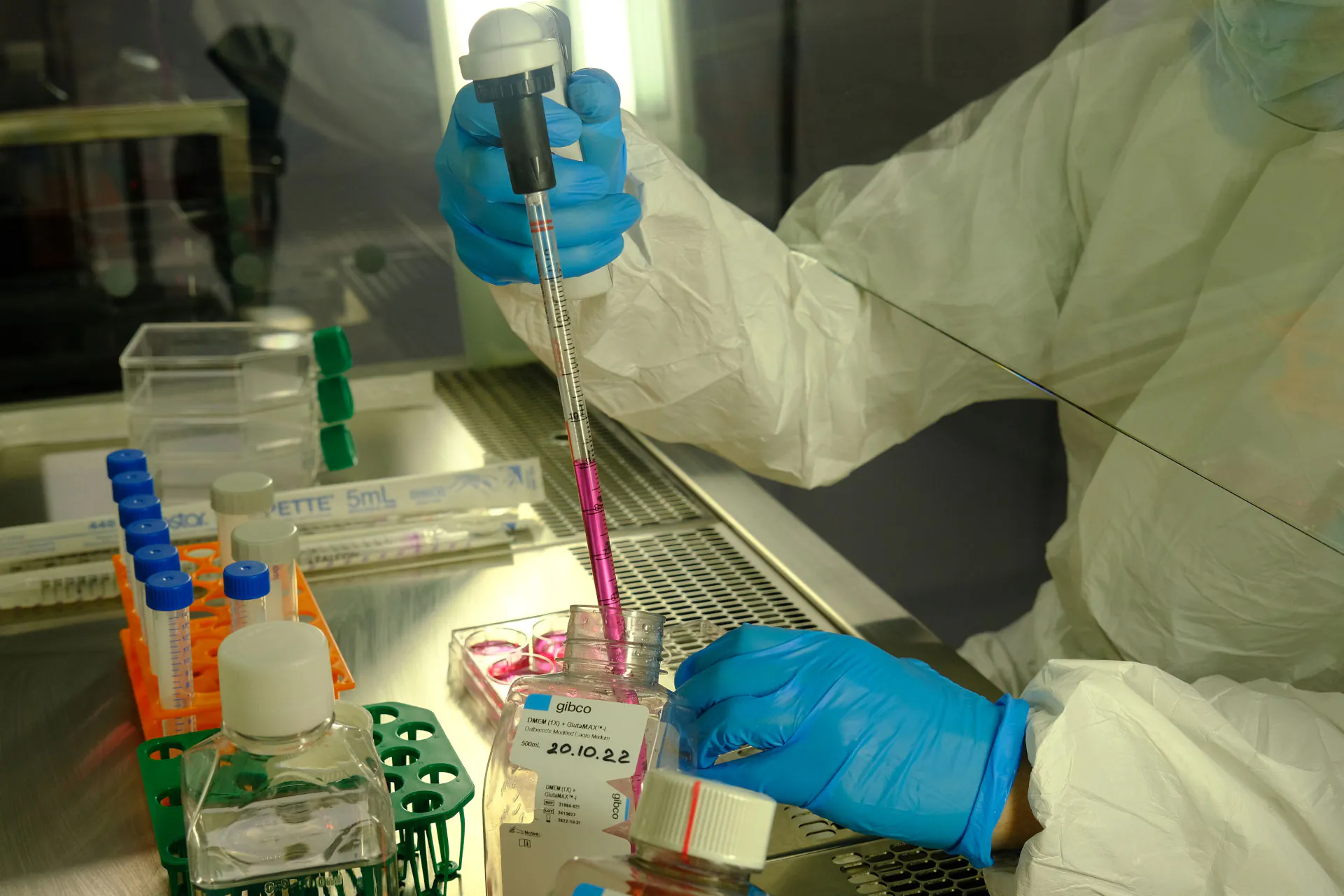
Отделение клинической иммунологии
Отделение клинической иммунологии МРНЦ имени А.Ф. Цыба ежегодно выполняет от 60 до 80 тысяч иммунологических и серологических исследований. Проводится иммунофенотипирование (многопараметровая проточная цитометрия) с целью установления иммунологического варианта острого лейкоза или периферических лимфом. Проводится иммунологический контроль эффективности лекарственной терапии у онкологических больных. Осуществляется иммунологический мониторинг стволовых клеток при стимуляции кроветворения в процессе подготовки больного к сбору стволовых кроветворных клеток для трансплантации. Выполняется оценка характера нарушений иммунитета и динамики ответа иммунной системы на проводимое лечение. Проводится диагностика групповой принадлежности крови.
- Многолетний опыт
- Запатентованные технологии
- Иммунодиагностика
- Гарантия качества
Диагностические исследования
- Иммунофенотипирование лейкозов, лимфом и миеломной болезни
- Определение минимальной остаточной болезни (МОБ) на этапах и по завершении лечения онкогематологических заболеваний
- Определение циркулирующих опухолевых клеток (ЦОК) в крови
- Определение диссеминированных опухолевых клеток (ДОК) в костном мозге, лимфоузлах, биологических жидкостях
- Определение количества стволовых CD34+ кроветворных клеток
- Определение и характеристика субпопуляций гемопоэтических и мезенхимальных стволовых клеток
- Иммунофенотипирование первичных культур лимфоидных клеток
- Иммунофенотипирование первичных культур опухолевых клеток
- Оценка количественного и функционального состояния клеточного и гуморального иммунитета
- Оценка цитокинового профиля
- Проведение цитотоксических тестов
- Определение групповой принадлежности крови и аутоантител
- Иммунологическая диагностика инфекций
- Биологический контроль качества (стерильность и апирогенность) лекарственных и радиофармацевтических препаратов
- Проведение аллергопроб
Иммунологические методы диагностики и лечения — это неотъемлемая часть современного лечебного процесса в онкологии
ГРУППА «ОнкоБиоБанк»
- Хранение биоматериала
- 500 000 образцов онкоклеток пациентов
- 2000 образцов стволовых клеток
- Исследовательские программы
«ОнкоБиоБанк» — абсолютно необходимый ресурс для клинических трансплантационных и масштабных научно-исследовательских задач и целей.
«ОнкоБиоБанк» располагает:
- Полнофункциональным замораживателем S Y-LAB
- Морозильниками вертикальными с температурным диапазоном от −50 до −86 °С
- Морозильниками горизонтальными с температурным диапазоном до 150 °С
- Системой хранения в парах жидкого азота Biosafe
- Резервуаром Apollo для хранения и автоматической подачи жидкого азота — 350 л
- Программным обеспечением FreezerPro
- Единой электронной базой данных историй болезней и анамнезов онкопациентов
- «ОнкоБиоБанк» МРНЦ им. А.Ф. Цыба является научным центром, где возможно проведение крупных исследовательских проектов, и является уникальным источником информации
Адоптивная иммунотерапия
В течение последних десятилетий к базисным направлениям лечения рака (хирургическое вмешательство, лучевая терапия, лекарственная терапия) добавляются перспективные методы лечения — иммунотерапия. Иммунотерапия основывается на использовании разработок, направленных на восстановление нарушенных функций иммунной системы: стимуляции сниженного противоопухолевого иммунного ответа и блокировании супрессорных механизмов, способствующих опухолевому росту. Методы иммунотерапии всесторонне улучшают иммунитет, способствуя продлению срока безрецидивного течения заболевания, сокращению сроков восстановления после хирургического лечения и повышению качества жизни пациентов. Адоптивная клеточная иммунотерапия может быть реализована посредством применения любых клеток иммунной системы (Т-клетки, NK-клетки, дендритные клетки, макрофаги) — как просто активированных, так и генно-модифицированных.
Адоптивная иммунотерапия цитокин-активированными лимфоцитами
Персонализированный вид неспецифической клеточной иммунотерапии активированными лимфоцитами. При данной методике иммунные клетки забираются из периферической крови пациента и обрабатываются цитокинами для повышения их функциональной активности. Затем клетки возвращаются пациенту, что приводит к активации различных звеньев иммунитета, усилению иммунного ответа в отношении злокачественной опухоли, преодолению существующей опухолевой иммуносупрессии, снижению выраженности болевого синдрома, улучшению качества жизни онкологического больного.
- Эксклюзивная уникальная методика
- Применима на всех этапах лечения
- Без противопоказаний
- Эффективна в случае диссеминированного процесса
Вопрос о назначении адоптивной иммунотерапии рассматривается в каждом случае индивидуально в составе консилиума врачей-специалистов. Проведение данного вида клеточной иммунотерапии возможно как в амбулаторных условиях, так и в условиях стационара.
Дополнительными методами адоптивной клеточной иммунотерапии в онкологической практике являются: опухоль-ассоциированные антигенные вакцины (вакцины на основе дендритных клеток, МРНК-вакцины), ex vivo модифицированные аутологичные иммунокомпетентные клетки и клеточная терапия на основе химерных антигенных рецепторов (CAR-T, CAR-NK).
Разработка, производство и контроль качества иммунотерапевтических препаратов и клеточных продуктов осуществляются в условиях, соответствующих надлежащей производственной практике (GMP), что гарантирует безопасность, эффективность и качество лекарственных средств и биологических материалов, предназначенных для применения в клинических исследованиях и лечебной практике. Соблюдение принципов GMP включает в себя строгий контроль всех этапов процесса, от исходных материалов до готовой продукции, а также валидацию технологических процессов и регулярный аудит для обеспечения соответствия установленным стандартам качества и безопасности.
NK-клетки — киллеры
NK-клетки (естественные клетки-киллеры) — это особая популяция клеток крови, способная уничтожить опухолевую клетку (развивается так называемый цитотоксический эффект). Данные клетки составляют не более 10–15% среди всех лимфоцитов. С использованием специальных методик количество NK-клеток может быть значительно увеличено, и их введение пациенту позволяет добиться усиления противоопухолевого эффекта.
Благодаря запатентованной технологии адоптивной иммунотерапии проводится in vitro активация клеток иммунной системы (Т-клетки, NKT-лимфоциты, NK-клетки) с использованием цитокин-активированных лимфоцитов, естественных киллеров (NK-клетки).
Этапы лечения
Процедура получения активированных клеток иммунной системы включает в себя следующие этапы:
- У больного/донора забирается венозная периферическая кровь.
- Из периферической крови в стерильных условиях выделяются мононуклеарные клетки.
- С учетом количества этих клеток они помещаются в полную питательную среду с добавлением IL-2 и IL-15 и инкубируются в течение 14 дней в термостате.
- Ежедневно осуществляется контроль эффективности роста и активации иммунных клеток в суспензионной культуре, проводится оценка морфологии клеточных культур.
- Осуществляется контроль на стерильность препарата.
- Оценивается жизнеспособность и функциональная активность клеток.
- Каждые 72 часа культивирования часть суспензионных цитокин-активированных иммунных клеток в количестве от 2 до 10 млн собирается и вводится пациенту паравертебрально внутрикожно в 2–4 точки.
- Введение клеток стандартно осуществляется на 3, 5, 7, 9 и 11 дни, далее лечение продолжается по индивидуальной схеме без длительных перерывов.
- При необходимости часть активированных клеток помещается на хранение в жидкий азот (ОнкоБиоБанк).
Вакцины на основе дендритных клеток
С 2024 года на базе отделения реализуется такой вид сопроводительной адоптивной клеточной терапии, как использование клеточных продуктов на основе дендритных клеток (дендритно-клеточные вакцины).
Дендритные клетки (ДК) — мощные антигенпрезентирующие клетки иммунной системы, способные инициировать и модулировать противоопухолевый иммунный ответ.
Дендритные клеточные вакцины представляют собой терапевтический подход, основанный на использовании ex vivo обработанных ДК, нагруженных опухолевыми антигенами. Эти антигены могут быть получены из опухолевой ткани пациента, клеточных линий раковых клеток или синтезированы искусственно.
После культивирования и загрузки антигенами ДК вводят пациенту, стимулируя его иммунную систему к распознаванию и уничтожению опухолевых клеток.
Технологические аспекты производства дендритноклеточных вакцин
Производство дендритноклеточных вакцин начинается с получения не менее 50 мл венозной крови у пациента, за которым следует процедура фракционирования и выделения мононуклеарных клеток. Этот этап осуществляется в контролируемых лабораторных условиях, что является критически важным для получения функционально активных клеток. Затем мононуклеарные клетки подвергают воздействию цитокинов, в результате чего получают зрелые дендритные клетки (ДК).
После получения ДК их «нагружают» опухолевыми антигенами. Важным аспектом является то, что источником этих антигенов служат непосредственно опухолевые клетки самого пациента, которые выделяются из биопсийного материала. Важно, чтобы фрагмент опухоли не подвергался химической обработке (погружение в формалин) и заливке в парафин, иначе получить функционально активные антигены будет невозможно. Такой аутологичный подход обеспечивает уникальный и более обширный спектр потенциально иммуногенных пептидов (фрагментов опухолевых белков) для каждого конкретного больного, что является значимым преимуществом, поскольку учитывает индивидуальные особенности раковой опухоли.
Терапия на основе мезенхимальных стволовых клеток
Еще одним направлением работы подразделения является терапия с применением стволовых мезенхимальных/стромальных клеток костного мозга. Исследования в данной области были начаты профессором А.Г. Коноплянниковым, когда было получено разрешение на проведение трансплантации кардиомиобластов, полученных из мезенхимальных стволовых клеток (МСК), при ишемиях различного происхождения.
МСК — это уникальная популяция клеток, способная восстанавливать большинство тканей организма, что делает эти клетки универсальным объектом регенеративной медицины. Данные мультипотентные негемопоэтические клетки-предшественники способны дифференцироваться в клетки разных типов тканей взрослого организма, в том числе в жировую, мышечную, клетки сосудистого эпителия, нервные клетки и кардиомиоциты. Центр располагает опытом более 1000 успешных трансплантаций МСК, большинство из которых проводились с целью снижения последствий ишемии сердца.
Особенности методики:
- Культуру МСК вводят капельно внутривенно в дозе 1,5–2 млн на 1 кг массы тела.
- Для системной трансплантации 120–160 млн аллогенных МСК, размноженных в культуре, клетки взвешивают в 200 мл стерильного физиологического раствора и вводят пациенту в течение 40–60 минут.
Исследования
Проводятся экспериментальные исследования по изучению возможности использования МСК для клеточной терапии при различных заболеваниях.
Например:
Применение МСК в комплексной терапии пациентов с хронической сердечной недостаточностью — системная (внутривенная) трансплантация кардиомиобластов, полученных из МСК аутологичного костного мозга. Показано, что методика минимально инвазивна, не вызывает осложнений.
Исследование эффективности введения МСК как 4–6-й линии терапии рефрактерной реакции «трансплантат против хозяина» (РТПХ), сопровождаемой гипофункцией трансплантата.
О лаборатории клинической иммунологии
В 60–70-е годы ХХ века лаборатория радиационной иммунологии, возглавляемая д.м.н., проф. К.П. Кашкиным, входила в состав отдела радиобиологии экспериментального сектора Института медицинской радиологии АМН СССР (ИМР АМН СССР). В 1978–1984 гг. лабораторией руководил известный российский ученый-иммунолог д.м.н. А.А. Ярилин, а с 1985 г. — д.м.н. Б.П. Суринов. В связи с необходимостью проведения иммунологических исследований в онкологической практической медицине в 1990 г. из нее была выделена лаборатория клинической иммунологии, вошедшая в структуру клинического сектора ИМР АМН СССР в качестве самостоятельного подразделения. С 1990 по 2019 г. его деятельность возглавляла к.б.н. Е.Г. Кузьмина. В 2012 г. лаборатория была введена в отдел клинической лабораторной диагностики МРНЦ им. А.Ф. Цыба, объединивший также отделения лабораторной диагностики и «ин витро» радионуклидной диагностики (зав. отделом к.б.н. М.В. Полуэктова). В настоящее время создано отделение клинической иммунологии (руководитель д.б.н. Л.Ю. Гривцова), в функции которого входят как иммунологическая диагностика опухолей, так и разработка инновационных иммунотерапевтических методов, направленных на эрадикацию (полное излечение) рака.