Исследования, научные проекты и инновации в МГС МНИОИ им. П.А. Герцена направлены на развитие персонализированной онкологии и внедрение передовых молекулярно-генетических технологий в клиническую практику. Работа отдела объединяет фундаментальные исследования, прикладные разработки и трансляцию научных результатов в диагностику и лечение злокачественных новообразований. Особое внимание уделяется мРНК-вакцинам, фармакогеномике, биоинформатике и созданию отечественных диагностических решений, формирующих основу медицины будущего.
Наши разработки
В МГС МНИОИ им. П.А. Герцена выполняются государственные задания и грантовые проекты. За последние пять лет сотрудники отдела создали обширный пул публикаций, отражающих высокий научный уровень и качество работы.
Разработка мРНК вакцины
мРНК-вакцины являются одной из наиболее передовых и перспективных разработок в лечении онкологических заболеваний, обеспечивая индивидуализированный подход к терапии рака. В настоящее время МГС участвует в разработке технологии мРНК-вакцины для лечения пациентов с меланомой и другими типами злокачественных новообразований (ЗНО). Эта вакцина является результатом сотрудничества 17 ведущих научно-исследовательских институтов, включая Национальный медицинский исследовательский центр радиологии.
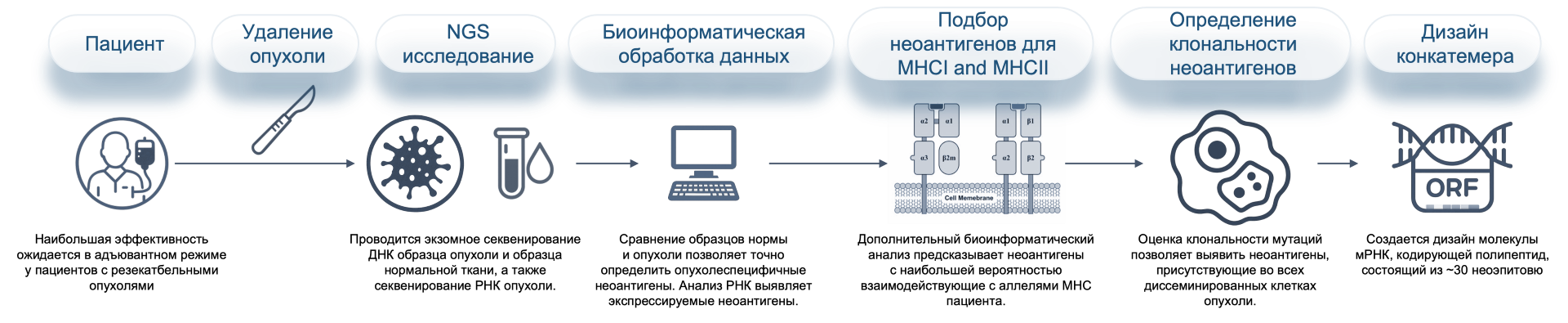
МГС отвечает за персонализированный подбор неоантигенных пептидов — ключевой элемент в разработке мРНК- вакцин. Этот процесс начинается с секвенирования ДНК и РНК опухолевых клеток и крови пациента для выявления специфических мутаций. Далее с помощью биоинформатических методов отбираются наиболее перспективные неоантигенные пептиды. Эти пептиды должны быть способны связываться с молекулами главного комплекса гистосовместимости (ГКГ) и быть представленными на поверхности опухолевых клеток, чтобы их могли распознать Т-клетки иммунной системы
В частности, происходит активная разработка персонализированных мРНК-вакцин в сотрудничестве с Центром Гамалеи.
Разработка велась с 2024 года, в декабре 2025 было получено разрешение на клиническое применение
В рамках разработки этого процесса были завершены 3 проекта:
- Разработано программное обеспечение для идентификации неоантигенных пептидных последовательностей и создания на их основе конкатемера для конструирования мРНК-вакцины в модели меланомы мышей
- Разработан прототип неоантигенспецифической мРНК-вакцины для лечения трижды негативного рака молочной железы
- Разработан экспериментальный образец программного комплекса для отбора наиболее перспективных неоантигенов для персонализированного лечения рака с использованием мРНК-вакцин
В 2025 году было получено разрешение на применение разработанного набора для подбора биотехнологических препаратов
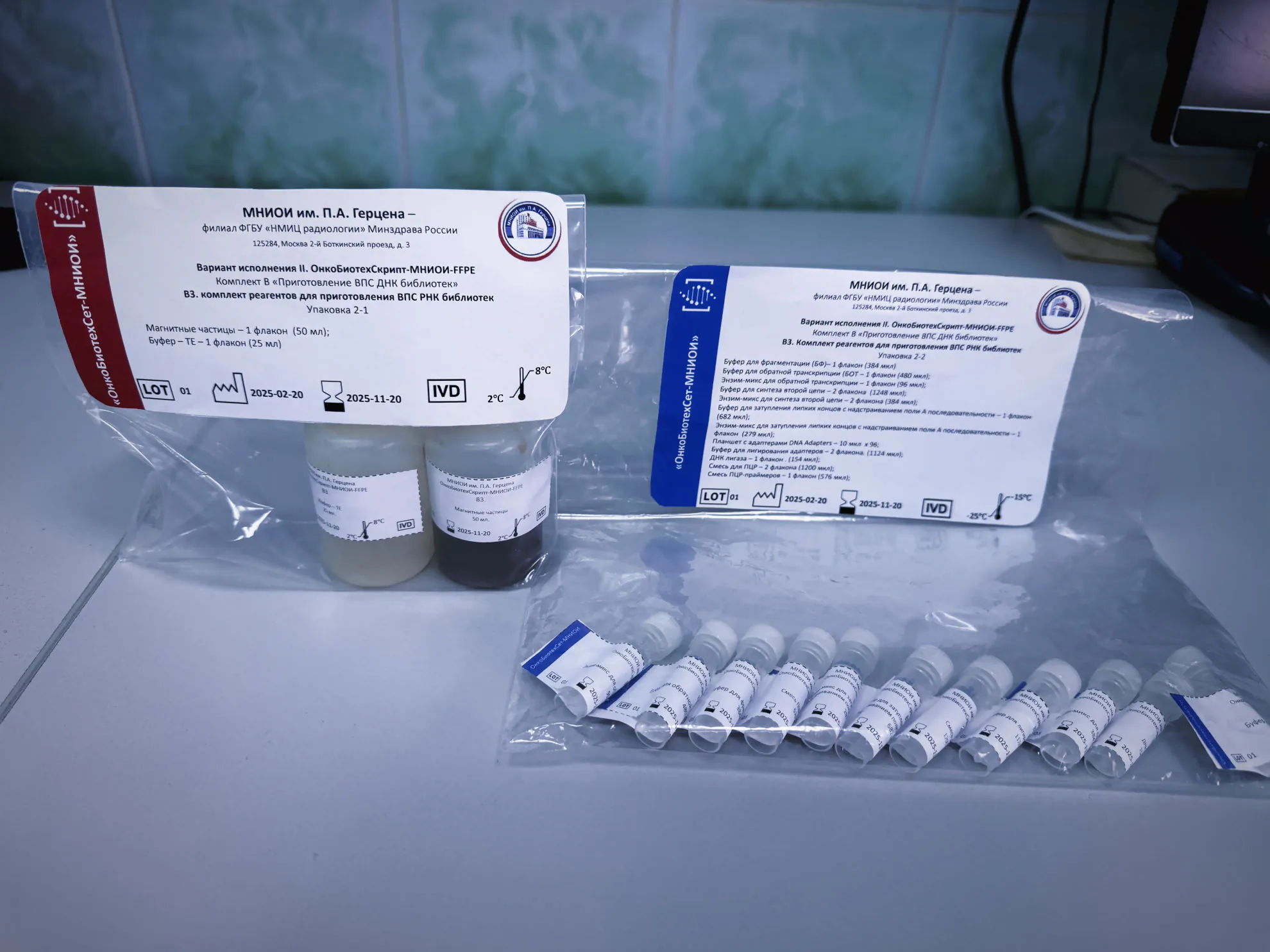
Приказом Росздравнадзора от 06.08.2025 № 4720 предоставлено разрешение на применение незарегистрированного медицинского изделия для диагностики in vitro «Набор реагентов с программным обеспечением для подбора противоопухолевой лекарственной терапии, в том числе мРНК вакцин, и других биотехнологических лекарственных препаратов (БТЛП), производимых по индивидуальному назначению на основании результатов генетических исследований (Онко БиотехСет-МНИОИ)», производства ФГБУ «НМИЦ радиологии» Минздрава России, № Р012-00110-77/02871296, дата предоставления разрешения 06.08.2025.
Комплекс для in vitro диагностики злокачественных новообразований состоит из:
- лабораторных реагентных наборов;
- вычислительного ПО для анализа секвенирования;
- модулей интерпретации для подбора терапии.
- Объединяет молекулярно-генетический анализ и клиническую интерпретацию в едином цикле.

Дальнейшие планы на 2026
20 ноября 2025 стало известно об одобрении Минздравом вакцины на платформе мРНК для лечения меланомы (НЕООНКОВАК)
в 2026 году в России начнётся экспериментальное лечение мРНК-вакциной больных меланомой
Механизм действия противораковых мРНК вакцин
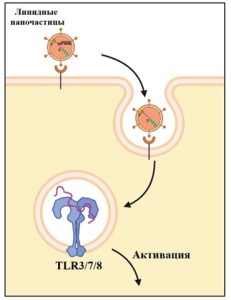
После эндоцитоза мРНК попадает в цитоплазму антигенпрезентирующей, например, дендритной клетки, где может быть распознана эндосомальными Toll-подобными рецепторами (TLR3/7/8), что приводит к активации клетки и выработке цитокинов и хемокинов, таких как IL-6, IL-2 и TNF-α, способствующих активации наивных Т-клеток.
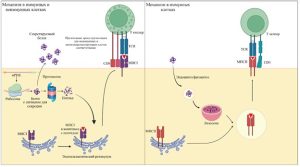
После проникновения мРНК в цитоплазму как иммунных, так и неиммунных клеток, она транслируется рибосомами в неоантигенный белок. Этот белок расщепляется протеасомой на пептидные эпитопы, которые далее презентуются на поверхности клеток в комплексе с молекулами MHCI. В антиген-презентирующих клетках (АПК) в зависимости от конструкторских особенностей мРНК возможен дополнительный транспорт антигенов из цитоплазмы в лизосомы с последующим расщеплением и презентацией через MHC-II, что обеспечивает активацию как CD8+, так и CD4+ Т-клеточного ответа.
Если в конструкции мРНК предусмотрен сигнал секреции, то продуцируемый неоантигенный белок может покидать клетку. Эти белки захватываются антиген-презентирующими клетками (АПК), например, дендритными клетками, через процессы эндо- или фагоцитоза и презентуются CD4+ Т-клеткам посредством MHC-II, что инициирует Т-хелперный и гуморальный иммунный ответы. Кроме того, экзогенные пептиды в комплексе с MHC-I могут быть представлены CD8+ Т-клеткам через кросс-презентацию, способствуя активации цитотоксических Т-клеток. Такой механизм позволяет вызвать комплексный и эффективный иммунный ответ против опухолеспецифичных антигенов
Разработка тест систем для онкодиагностики
Разработка тест-системы для диагностики частых мутаций гена PIK3CA методом ПЦР
Выполняется госзадание по теме “Разработка оригинальной тест-системы для диагностики частых мутаций гена PIK3CA методом ПЦР в режиме реального времени, направленной на диагностику рака молочной железы, в том числе метастатического, и выявление мишеней для проведения таргетной терапии”
Статья:
П.А. Шаталов, Е.М. Веселовский, А.А. Траспов, Е.А. Кириллова, М.А. Ревкова, Д.В. Багдасарова, И.А. Леухина, А.П. Шинкаркина, М.П. Райгородская, А.В. Мурзаева,Ю.А. Меченичи, П.В. Мишакова, А.Д. Каприн, П.В. Шегай. Распространенность клинически значимых мутаций PIK3CA: результаты анализа опухолевых образцов 1452 пациентов российской когорты. Онкология. Журнал им. П.А. Герцена. 2025, Т. 14, №6, с. 1–7 https://doi.org/10.17116/onkolog2025140611
Фармакогеномная платформа
Ариадна ссылка
Участие в создание фармакогеномной платформы для поддержки принятия персонализированных врачебных решений в онкологии. Эта платформа разработана с применение алгоритмов машинного обучения в биоинформатических конвейерах и она позволяет аккумулировать и хранить не только геномные данные больных и сведения об ассоциациях «биомаркер — лекарственный препарат», но и массив клинико-фенотипической информации. Это является важным этапом для дальнейшего анализа и поиска факторов, способных определять ответ на проводимое противоопухолевое лечение
Статьи:
Шаталов П.А., Райгородская М.П., Шинкаркина А.П., Мурзаева А.В., Макарчук В.М., Аверинская Д.А., Траспов А.А., Каприн А.Д., Шегай П.В. Роль фармакогеномики в персонифицированном лечении онкологических заболеваний.
Онкология. Журнал им. П.А. Герцена. 2023. Т. 12. № 6. С. 75-81. 10.17116/onkolog20231206175
Шаталов П.А., Веселовский Е.М., Райгородская М.П., и др. Интеграция NGS-тестирования со стандартными методами молекулярно-генетических исследований в онкологии. Онкология. Журнал им. П.А. Герцена. 2024;13(6):84‑90.
Doi:10.17116/onkolog20241306184
Участие в создании референсного генома человека.
Отделение молекулярно-генетической службы принимало участие в создании первого российского эталонного генома человека, обозначенного как E701, разработанного в результате совместных усилий четырёх ведущих научных лабораторий.
Статья:
Iuliia Vasiliadis, Vera Belova, Anna Shmitko, Anna Kuznetsova, Alina Samitova, Oleg Suchalko, Andrey Goltsov, Peter Shatalov, Peter Shegai, Elena Kulyabina, Tatiana Kulyabina, Olga Melkova, Denis Rebrikov, Dmitriy Korostin. Experience in developing the human genome standard E701, NAR Genomics and Bioinformatics. Volume 7, Issue 2, June 2025.
https://doi.org/10.1093/nargab/lqaf057
Сравнительный анализ 4-х наборов для экзомного секвенирования
МГС участвовала в изучении и сравнении четыре доступных в 2024 году набора для экзомного обогащения: Agilent SureSelect Human All Exon v8, Roche KAPA HyperExome, Vazyme VAHTS Target Capture и NEXome Plus Panel v1. Их оценка производилась по различным метрикам, включая качество покрытия, равномерность чтения, эффективность выявления вариантов и практическую применимость в клинической диагностике. Набор NEXome Plus Panel v1 продемонстрировал наивысшую точность с наименьшим количеством ложноположительных результатов, но с несколько более низкой F-мерой, чем другие наборы.
Статья:
Belova V, Vasiliadis I, Repinskaia Z, Samitova A, Shmitko A, Ponikarovskaya N, Suchalko O, Cheranev V, Peter S, Peter S, Andrey K, Rebrikov D, Korostin D. Comparative evaluation of four exome enrichment solutions in 2024: Agilent, Roche, Vazyme and Nanodigmbio. BMC Genomics. 2025 Jan 27;26(1):76. doi: 10.1186/s12864-024-11196-z. PMID: 39871131; PMCID: PMC11770928.